各藥品生產(chǎn)企業(yè)及配送企業(yè):
為滿(mǎn)足我院臨床診療需求���,擬啟動(dòng)我院2024年新藥遴選工作����。為更好地了解市場(chǎng)上藥品相關(guān)信息���,并作為后續(xù)新藥遴選的參考���,現(xiàn)開(kāi)展新藥遴選市場(chǎng)信息調(diào)研,相關(guān)事宜公告如下:
一���、新藥定義
新藥是指國(guó)家相關(guān)部門(mén)批準(zhǔn)同意生產(chǎn)使用���,且初次進(jìn)入我院《基本用藥目錄》;在安全性�����、有效性��、經(jīng)濟(jì)性等方面有顯著特點(diǎn)�,且能提升我院現(xiàn)有藥物治療水平的藥品。
申報(bào)的品種與醫(yī)院常購(gòu)藥品通用名相同�����,但規(guī)格或劑型不同的品種�����,視為新藥����。
二、新藥引進(jìn)原則
(一)依據(jù)安全���、有效��、經(jīng)濟(jì)的用藥原則和醫(yī)院疾病治療特點(diǎn)�����,優(yōu)化醫(yī)院用藥目錄�����。促進(jìn)基本藥物優(yōu)先配備使用�����,形成以基本藥物為主導(dǎo)的“1+X”用藥模式�。“1”為國(guó)家基本藥物目錄����;“X”為非基本藥物,經(jīng)醫(yī)院藥委會(huì)充分評(píng)估論證���,優(yōu)先選擇國(guó)家組織集中采購(gòu)藥品�、國(guó)家醫(yī)保目錄藥品��、國(guó)家談判藥品�。
(二)醫(yī)院《基本用藥目錄》當(dāng)中,口服劑型與注射劑型各不超過(guò)“一品兩規(guī)”(兒童用藥劑型除外)���。
三����、申報(bào)基本原則
(一)屬于“四川醫(yī)保公共服務(wù)——藥品和醫(yī)用耗材招采管理系統(tǒng)”(以下簡(jiǎn)稱(chēng)平臺(tái))掛網(wǎng)品種。
(二)同一生產(chǎn)企業(yè)限報(bào)2個(gè)品規(guī)��,若超額申報(bào)�����,所有申報(bào)視為“無(wú)效”����。
(三)“中成藥”只接收國(guó)藥準(zhǔn)字號(hào)為“Z”�����,且至少滿(mǎn)足“國(guó)家Ⅰ類(lèi)新藥”“國(guó)家談判品種”或“獲得省科技進(jìn)步一等獎(jiǎng)及以上科技獎(jiǎng)勵(lì)”條件之一的品種��。
(四)不接受紅黃區(qū)的藥品信息����。
四、申報(bào)資料
生產(chǎn)企業(yè)或其委托的配送企業(yè)提交申請(qǐng)資料:
(一)《新藥申請(qǐng)表》�����。
(二)生產(chǎn)企業(yè)提供營(yíng)業(yè)執(zhí)照復(fù)印件�����、藥品生產(chǎn)許可證復(fù)印件。全進(jìn)口藥品提供全國(guó)總代理營(yíng)業(yè)執(zhí)照復(fù)印件�����、藥品經(jīng)營(yíng)許可證復(fù)印件���。所有復(fù)印件需加蓋生產(chǎn)企業(yè)或全國(guó)總代理鮮章�。
(三)平臺(tái)掛網(wǎng)頁(yè)面打印件(需顯示掛網(wǎng)價(jià)�、醫(yī)保屬性、紅黃綠價(jià)格區(qū)間���、基藥屬性����、是否集采中選品種��、是否國(guó)家談判藥品���;需清晰并蓋企業(yè)鮮章)��。
(四)經(jīng)國(guó)家食品藥品監(jiān)督管理局(SFDA)批準(zhǔn)的法定藥品說(shuō)明書(shū)���。
(五)新藥申報(bào)承諾書(shū)��。
(六)產(chǎn)品介紹資料(臨床研究�、臨床指南等)����。
(七)申報(bào)藥品如系四川大學(xué)華西醫(yī)院�����、四川大學(xué)華西第二醫(yī)院����、四川大學(xué)華西口腔醫(yī)院及四川省人民醫(yī)院在用品種,提供申報(bào)藥品的配送協(xié)議或藥品銷(xiāo)售出庫(kù)單�。
(八)法人授權(quán)委托書(shū)(生產(chǎn)企業(yè)對(duì)配送企業(yè)授權(quán))
(九)法人授權(quán)委托書(shū)(供應(yīng)商對(duì)代理人授權(quán))
五、申報(bào)要求
(一)各企業(yè)應(yīng)真實(shí)����、準(zhǔn)確、規(guī)范填寫(xiě)資料�。如資料填寫(xiě)不全或填寫(xiě)錯(cuò)誤者,不接受更正�,視為無(wú)效資料����。
(二)除企業(yè)證照加蓋生產(chǎn)企業(yè)(或全國(guó)總代理)鮮章外�����,余資料均加蓋申報(bào)企業(yè)鮮章即可��。同一類(lèi)別資料頁(yè)碼較多者����,加蓋騎縫章。
(三)所有提交資料須真實(shí)有效�,各類(lèi)資料按要求整理匯編成冊(cè)。
(四)各相關(guān)企業(yè)不得直接與臨床科室及醫(yī)生聯(lián)系���,一經(jīng)核實(shí)����,將取消該企業(yè)參與資格�。
六、資料接收
(一)接收資料內(nèi)容:
1.新藥信息匯總表(附件1)���,接收可編輯的Excel版本����。
2.新藥市場(chǎng)調(diào)研申報(bào)書(shū)(附件2):按照附件2的順序?qū)①Y料整理,并轉(zhuǎn)換為PDF版本�。
(二)接收方式:
僅接收附件1和附件2的電子版資料。將上述資料發(fā)送到指定郵箱ypcgzyy@163.com����。主題:藥品名-劑型-規(guī)格。資料以附件形式按要求上傳��,如圖: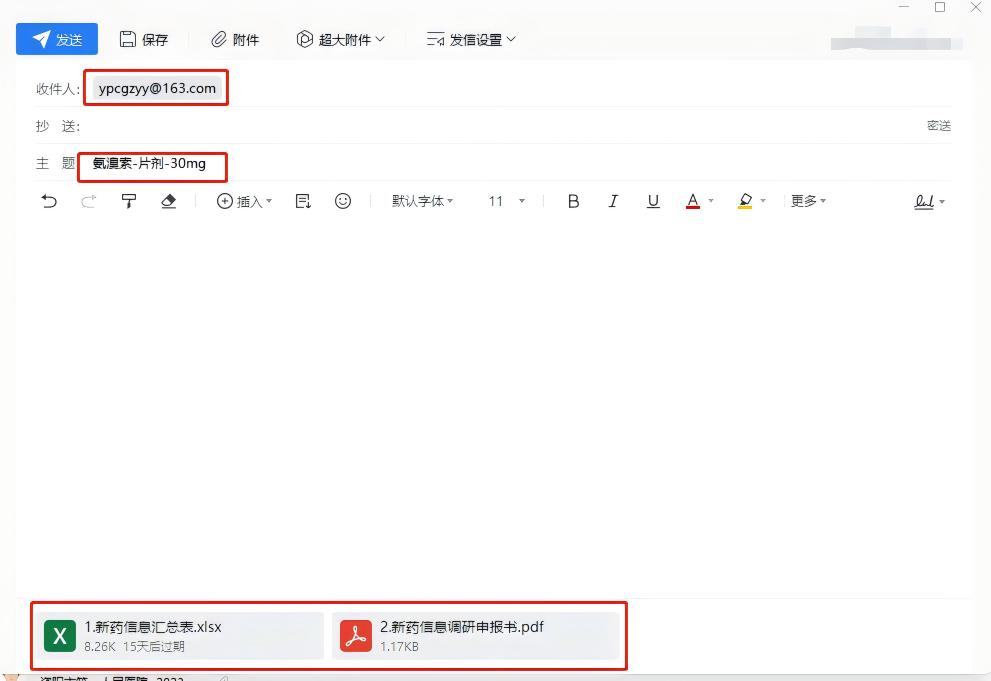
(三)接收時(shí)間:2024年10月12日-10月18日����。
七�、其他
(一)聯(lián)系人及聯(lián)系方式:黃老師,028-26578063��。
(二)以上內(nèi)容解釋權(quán)歸資陽(yáng)市中心醫(yī)院藥事管理與藥物治療學(xué)委員會(huì)所有����。?
資陽(yáng)市中心醫(yī)院
2024年10月12日